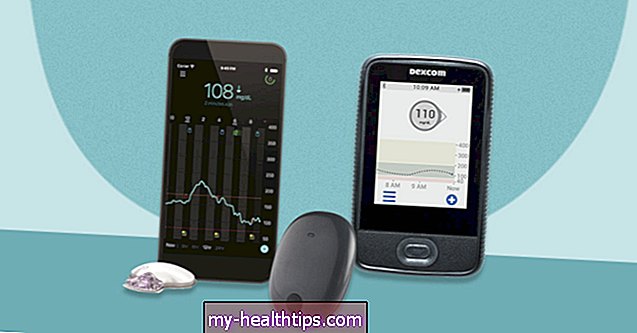
To wielka wiadomość w przestrzeni technologicznej społeczności diabetologicznej, ponieważ FDA przyznała, jak nazywa to „przełomowe urządzenie”, przyszłemu systemowi z zamkniętą pętlą, który łączy ciągły monitor glukozy z pompą insulinową, aby konkurować z bezdętkowym Omnipodem.
14 marca FDA nadała południowokoreańskiej firmie EoFlow to przyspieszone oznaczenie dla jej systemu automatycznego dostarczania insuliny (AID) o nazwie EoPancreas. To już czwarty raz, kiedy FDA przyznała nowemu przełomowemu urządzeniu systemowi zamkniętej pętli cukrzycowej od czasu jego utworzenia w 2016 r. - firma Bigfoot Biomedical otrzymała ją w listopadzie 2017 r. Za przyszłą technologię AID, a Medtronic otrzymała ją z aprobatą pediatryczną Minimed 670G. latem ubiegłego roku, a następnie ponownie w lutym 2019 r. w celu stworzenia przyszłego „spersonalizowanego systemu zamkniętego”, firma rozwija.
Chociaż EoFlow nie jest tak dobrze znany jak niektóre inne w tej przestrzeni, jest to firma, którą widzieliśmy przez lata, prezentującą swoją pompę łatek i połączoną z nią aplikację mobilną na konferencjach, takich jak doroczne sesje naukowe ADA. Sama pompa bezdętkowa nazywa się EoPatch i plotka głosi, że pracowali nad CGM, ale do tej pory nie było dostępnych zbyt wielu szczegółów. JDRF współpracował z firmą kilka lat temu (po raz pierwszy sfinansował jakiekolwiek koreańskie badania w obiegu zamkniętym), a teraz świętuje dostęp do przyspieszonego procesu przeglądu regulacyjnego, który może przełożyć się na szybsze niż oczekiwano uruchomienie tutaj, w USA.
Oto, co wiemy o EoPancreas po rozmowie z prezesem EoFlow Luisem Malave (byłym dyrektorem Insulet ponad dekadę temu i dyrektorem badawczo-rozwojowym Minimed w latach 90.), a także informacje online:
Co to jest EoPancreas?

Dla tych, którzy wcześniej nie słyszeli o EoFlow, jest to południowokoreańska firma założona w 2011 roku, która ma teraz biuro w San Jose w Kalifornii. Jej założyciel i dyrektor generalny Jesse Kim prowadził startup półprzewodnikowy w Dolinie Krzemowej po ukończeniu MIT i ostatecznie założył EoFlow jako uniwersyteckie centrum inkubacji w Seulu. Od października 2017 roku Malave jest częścią zespołu pracującego w biurze w Kalifornii.
Ich zestaw produktów składających się na system EoPancreas obejmuje teraz:
Patch Pump: nazywana EoPatch, jest to prostokątna pompa insulinowa wielkości pagera, która przylega do skóry bez potrzeby stosowania plastikowych rurek, jak w przypadku tradycyjnych pomp. Jest w pełni jednorazowego użytku i wodoodporny, utrzymuje się na ciele przez 72 godziny i mieści do 200 jednostek insuliny. Projekt, który ostatecznie wejdzie na rynek, może się w pewnym stopniu różnić, ale współczynnik kształtu pozostaje w większości taki sam. Istniejąca pompa łatkowa EoFlow pierwszej generacji jest nieco cieńsza (przy 9,9 mm x 32,4 mm x 12,9 mm) niż OmniPod (39 mm x 52 mm x 14,5 mm). W EoPatch zastosowano również igłę ze stali nierdzewnej o średnicy 30 G, która pomaga zminimalizować okluzje (zatykanie). Ale ponieważ CGM byłby wbudowany w samą pompę łatkową, jest szansa, że doda trochę grubości, około pół centymetra, jak nam powiedziano. Malave mówi nam również, że spodziewają się, że najpierw uruchomią pompę łatek w Stanach Zjednoczonych, jako rodzaj pierwszej generacji, zanim dodadzą inteligentne algorytmy i ostatecznie wbudowaną technologię CGM.
Sterowanie odbiornikiem lub smartfonem: wersja EoPatch, która jest już dostępna w Korei, wykorzystuje do działania urządzenie przenośne, podobnie jak Personal Diabetes Manager (PDM) firmy OmniPod; na samej pompie nie ma przycisków. Według strony internetowej EoFlow, to, co pojawi się na rynku w Ameryce, będzie wymagało użycia specjalnego kontrolera ręcznego z interfejsem z kolorowym ekranem dotykowym - zablokowanym w stylu smartfona z Androidem. To, czy to urządzenie w stylu PDM jest tym, co widzimy, wypuszczonym na rynek z pełnym systemem EoPancreas, dopiero się okaże, ponieważ firma prawdopodobnie omawia kontrolę aplikacji na smartfony z regulatorami. Jest to już dyskusja, którą Insulet prowadzi z regulatorami dla swoich platform zamkniętej pętli nowej generacji OmniPod, więc wkrótce możemy zauważyć pewien ruch.
Czujnik CGM: nie ma zbyt wielu szczegółów publicznie, ale powiedziano nam, że EoPancreas zostanie zintegrowany z istniejącą technologią CGM. W szczególności firma osiągnęła porozumienie w sprawie używania czujnika CT-100B CGM wyprodukowanego przez chińską firmę POCTech, który widzieliśmy na konferencjach jako produkt „ja też”, który chwali się swoim „malutkim miękkim” czujnikiem 3 mm. i dokładność. Ten czujnik CGM zostanie wbudowany w pompę łatkową, chociaż Malave mówi nam, że ma również nadzieję na współpracę z innymi producentami CGM, aby mieć je jako opcje z systemem EoPancreas. Jak zauważono, czujnik POCTech CGM doda nieco grubości do ogólnego projektu urządzenia, mówi Malave. Biorąc pod uwagę nowe oznaczenie FDA „iCGM” (interoperacyjny CGM) przyznane jako pierwsze Dexcom G6, możemy sobie wyobrazić, dokąd EoPancreas ma nadzieję pójść w miarę postępów.
EoCloud: Podobnie jak większość połączonych systemów w dzisiejszych czasach, EoPancreas będzie oferować własne oprogramowanie w chmurze, które nazywa EoCloud. Spowoduje to wykorzystanie algorytmów sztucznej inteligencji (AI) działających na zastrzeżonej platformie do wykonywania obliczeń, które pomogą mu dowiedzieć się o każdym użytkowniku, umożliwiając dostosowanie sterowania w pętli zamkniętej dla każdego PWD (osoby z cukrzycą). Powiedziano nam, że inteligentne rozwiązania systemu będą oparte na algorytmie TypeZero Technologies licencjonowanym w 2018 roku przed przejęciem tej firmy przez producenta CGM Dexcom.
EoFlow spodziewa się, że dalsze dyskusje FDA będą miały miejsce w tym roku, biorąc pod uwagę przyznane niedawno „oznaczenie przełomowego urządzenia”, z próbami klinicznymi, które mają się odbyć w 2020 r. I przewidywanym komercyjnym uruchomieniem w pewnym momencie w 2021 r.
„Nasza firma ma trajektorię, z której jesteśmy podekscytowani” - powiedział Malave Cukrzyca. „Ludzie lubią mieć tylko jedną rzecz, którą muszą nosić, a wszystko odbywa się za pośrednictwem smartfona, bez którego po prostu nie możemy się obejść. To od nas, technologów, zależy, czy im to damy i zapewnimy im możliwość spersonalizowania tego, czego chcą ”.
„Przełomowe oznaczenie urządzenia” FDA
Program Przełomowych Urządzeń FDA przyznaje priorytetowy przegląd firmom z obiecującą nową technologią w opiece nad chorobami przewlekłymi. Uczestnikom przyznaje się priorytetową ocenę, wraz z „interaktywną komunikacją dotyczącą rozwoju urządzenia i protokołów badań klinicznych, aż do decyzji o komercjalizacji”. Utworzony właśnie w 2016 r. Nowy tytuł „nowatorskich, innowacyjnych” urządzeń został przyznany ok. 110 przedmiotom i jak dotąd zatwierdzono około 10 z nich.
W przestrzeni D, po Bigfoot Biomedical i Medtronic Diabetes, może wydawać się zaskakujące, że mało znana koreańska firma byłaby następną, która otrzymałaby to oznaczenie w konkurencyjnym wyścigu o wprowadzenie na rynek technologii „sztucznej trzustki”.
Szczerze mówiąc, nasz zespół zawsze przewracał oczami na EoFlow, widząc ich na konferencjach lub wspominanych przez lata. Wydaje się jednak, że JDRF wyprzedziło krzywą kilka lat temu, kiedy organizacja ogłosiła na początku 2017 r., Że będzie finansować część badań EoFlow - po raz pierwszy grupa T1D zainwestowała również w tę konkretną firmę o zamkniętym obiegu. jako pierwsza osoba, która sfinansowała koreańską firmę zajmującą się technologią diabetologiczną.
„Konstrukcje do noszenia nowej generacji, które są mniejsze i wykorzystują projekt zorientowany na użytkownika, usuwają bariery, które uniemożliwiają niektórym ludziom, zwłaszcza małym dzieciom, korzystanie z tych ratujących życie i zmieniających życie urządzeń do zarządzania glukozą” - powiedział dr Jaime Giraldo, naukowiec z JDRF. wtedy.
To, jak szybko ich produkty trafiają na rynek, jest w dużej mierze oparte na dyskusjach FDA, nawet przy tym szczególnym przełomowym statusie.
Poprosiliśmy FDA o więcej szczegółów na temat firm związanych z cukrzycą, które otrzymały to oznaczenie, ale powiedziano nam, że informacje są uważane za poufne w ramach procesu przeglądu i nie są udostępniane, chyba że firma zdecyduje się najpierw udostępnić te informacje. Jak wspomniano, wydaje się, że FDA przyznała do tej pory oznaczenie tylko czterem konkretnym systemom z obiegiem zamkniętym:
- Bigfoot Biomedical otrzymał oznaczenie w listopadzie 2017 r., Chociaż w tamtym czasie nadal był znany jako „Expedited Access Pathway”, zanim został przemianowany na proces Breakthrough Device Designation.
- Firma Medtronic otrzymała go w czerwcu 2018 r. Za zgodą swojego Minimed 670G dla dzieci w wieku 7-14 lat.
- W lutym 2019 roku firma Medtronic ponownie otrzymała to przełomowe, przyspieszone oznaczenie dla przyszłej technologii spersonalizowanej pętli zamkniętej - coś wykraczającego poza obecny system z większą automatyzacją i spersonalizowanymi aspektami.
- EoFlow dołącza do listy EoPancreas, która będzie obejmowała przegląd technologii firmy, w tym samej pompy łatkowej, początkową „inteligentną” wersję, a następnie ostatecznie zintegrowany system zamkniętej pętli CGM.
EoFlow's Malave twierdzi, że to oznaczenie prawne pozwoli firmie na stworzenie „jasnych kamieni milowych w projektowaniu i rozwoju” z FDA w celu „przyspieszenia naszej zdolności do komercjalizacji tej ważnej nowej technologii”.
Ważne jest, aby wiedzieć, że uzyskanie tego oznaczenia nie gwarantuje, że technologia każdej firmy będzie dostępna szybciej. ETA nie jest ustalonym, uniwersalnym harmonogramem, ponieważ zależy od technologii i dyskusji regulacyjnych. Ale to z pewnością stawia EoFlow w lepszej pozycji, aby dążyć do spodziewanego uruchomienia do 2021 r.
Nowe bezdętkowe pompy insulinowe i zamknięte pętle
EoFlow z pewnością nie jest jedynym graczem opracowującym nowy system zamkniętej pętli / AID / AP wykorzystujący bezdętkową „pompkę”. W opracowaniu jest znacznie więcej, w tym:
DiabeLoop: Ten francuski startup opracowuje DGLB1, hybrydowy system o zamkniętej pętli, który łączy CGM, pompę i zablokowany smartfon w celu sterowania. Ich pierwsza generacja będzie wykorzystywać wielokolorową hybrydową pompkę Kaleido z łatką, która jest małym prostokątem, który przykleja się do ciała i ma krótki tradycyjny przewód, który łączy się z zestawem infuzyjnym. Podczas gdy pompa Kaleido ma faktyczne przyciski, które mogą być używane do bezpośredniego dozowania, ich wersja z zamkniętą pętlą łączy się z systemem DiabeLoop na zablokowanym smartfonie (Sony Xperia Z1) i pobiera dane z Dexcom G6 CGM za pomocą algorytm podejmowania decyzji dotyczących dawkowania. Diabeloop współpracuje również z innymi partnerami, w tym hybrydową pompą rurkową CellNovo i może w pewnym momencie korzystać z tego urządzenia. (Zobacz nasze wcześniejsze relacje z DiabeLoop tutaj).
OmniPod Horizon: Chociaż myślimy również o premierze w 2021 r., Najprawdopodobniej wielu członków społeczności D jest bardzo podekscytowanych tym produktem nowej generacji od Insulet, producenta OmniPod! Oparty na obecnie uruchamianej platformie OmniPod DASH, która ma zintegrowaną technologię Bluetooth Low Energy, Horizon będzie wersją systemu zamkniętej pętli z pompką. Trwają próby rozwoju tej technologii.
Roche Solo: Ludzie prawie zrezygnowali z urządzenia pompy łatkowej Solo, które Roche nabył w 2010 roku. Pomimo, że urządzenie pierwszej generacji zostało już zatwierdzone przez FDA, Roche Diagnostics podjęła decyzję korporacyjną lata temu, aby go nie wprowadzać na rynek, ponieważ tak się nie stało. t zawierać zintegrowany monitor stężenia glukozy we krwi, taki jak OmniPod - decyzja wstrząsająca głową z perspektywy czasu. Jednak pozostał w fazie rozwoju firmy, aw 2018 roku Roche Wreszcie wprowadził mikro-pompę Solo w Europie. Jest to cienkie, pół-jednorazowe urządzenie, które jest tylko odrobinę większe niż OmniPod, ale przede wszystkim można je odłączać (!) I można bolusować bezpośrednio z małego zestawu patchowego Solo za pomocą wbudowanych przycisków. Roche pracuje również nad integracją technologii CGM, takiej jak wszczepialny system Eversense CGM, i ostatecznie uczyni tę część swojego własnego zamkniętego systemu w fazie rozwoju. Jeszcze nie widzieliśmy, żeby coś się zmaterializowało w USA, ale to nie znaczy, że firma nie przygotowuje się do złożenia tego tutaj.
Lilly Diabetes: Informowaliśmy, że Lilly pracuje nad własną technologią, hybrydową pompą z rurkami łatanymi, która przypomina okrągłą puszkę na tytoń, która mieści się w dłoni. Pharma Giant współpracuje z firmą Dexcom jako partner CGM i opracowuje to połączone urządzenie, które opisuje jako system automatycznego podawania insuliny, który „ostatecznie będzie miał funkcje zamkniętej pętli”. (zobacz nasze poprzednie relacje tutaj)
MiniPompa tandemowa „t: sport”: W przyszłości Tandem Diabetes Care opracuje mini pompkę, która jest ogólnie nieco mniejsza i ma mniejszy rozmiar wkładu niż zwykła pompa t: slim. Ekran zostanie wyeliminowany na rzecz bezpośredniego wyświetlania wszystkich danych na smartfonie. Będzie to jednorazowe urządzenie przyklejane do ciała, ale nie do końca pełna pompka, ponieważ nadal będzie potrzebować krótkiego czterocalowego złącza zestawu infuzyjnego (mini dren). Musieliśmy zobaczyć i trzymać prototyp tej mini pompy w połowie 2017 roku w siedzibie firmy Tandem w San Diego. Z obecną technologią Tandem Basal-IQ i zbliżającą się technologią zamkniętej pętli Control-IQ, które pojawią się pod koniec roku, nie ma wątpliwości, że ta przyszła minipompka będzie oferować ten sam typ funkcji zamkniętej pętli.
SFC Fluidics: JDRF nawiązał również współpracę z firmą SFC Fluidics z siedzibą w Arkansas, aby opracować system otwartej pętli z pompą i zamkniętą pętlą. Jak dotąd nie ma zbyt wielu szczegółów, ale SFC twierdzi, że opracuje „w pełni funkcjonalną pompę łatkową, która będzie działać na własnej platformie, a także opublikuje swój protokół komunikacyjny, aby zatwierdzone urządzenia mogły komunikować się z pompą łat”.
Poza tymi systemami pomp w fazie rozwoju i tymi, które należą do społeczności Do-It-Yourself #WeAreNotWaiting, która tworzy własne „zhakowane” wersje przy użyciu OmniPod, istnieją również inne systemy AID wykorzystujące tradycyjne rurkowe pompy insulinowe, w tym Medtronic, Tandem Diabetes, oraz takie jak:
Bigfoot Loop and Inject: Kalifornijski startup pracuje nad systemem automatycznego dostarczania insuliny (AID), który wewnętrznie nazywa Bigfoot Loop i Bigfoot Inject, w oparciu o wersję pompy, która będzie wykorzystywać nabytą technologię pompy Asante Snap, a także „Inteligentny wstrzykiwacz do insuliny”.
iLet Bionic Pancreas: Poza Bostonem, ta jest teraz pod parasolem start-upu Beta Bionics i będzie używać zestawu z dwoma hormonami do dawkowania zarówno insuliny, jak i glukagonu. Firma pracuje już nad prototypem czwartej generacji, który, jak nam powiedziano, będzie bardzo przypominał wersję komercyjną, która ma wejść na rynek w pewnym momencie w ciągu najbliższych 2-3 lat.
Cieszymy się, że WSZYSTKIE te potencjalne oferty w obiegu zamkniętym - zwłaszcza odmiany pomp płatkowych - oferują pacjentom duży wybór. Gratulacje dla EoFlow za wotum zaufania przez FDA.
Co więcej, doceniamy gotowość FDA do przyspieszenia działania firm, które umożliwiają tego typu technologie nowej generacji!




.jpg)










.jpg)