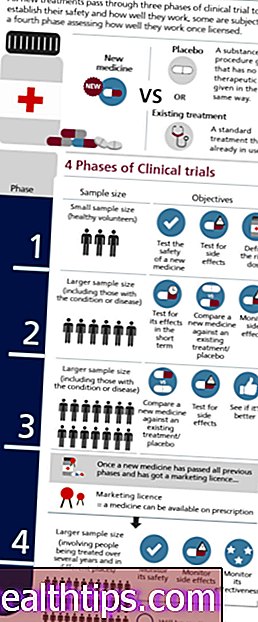
Większość badań klinicznych przebiega zgodnie z planem od początku do końca. Ale czasami próby są przerywane wcześniej. Na przykład Instytucjonalna Rada Rewizyjna i Rada ds. Monitorowania Danych i Bezpieczeństwa mogą przerwać badanie, jeśli uczestnicy doświadczają nieoczekiwanych i poważnych skutków ubocznych lub jeśli istnieją wyraźne dowody na to, że szkody przeważają nad korzyściami.
W niektórych przypadkach proces może zostać przerwany, ponieważ:
- Idzie bardzo dobrze. Jeśli na wczesnym etapie pojawią się wyraźne dowody na to, że nowa terapia lub interwencja jest skuteczna, badanie można wstrzymać, aby nowa terapia mogła być jak najszybciej szeroko dostępna.
- Nie można zrekrutować wystarczającej liczby pacjentów.
- Opublikowano wyniki innych badań, które odpowiadają na pytanie badawcze lub czynią je nieistotnymi.
Przedruk za zgodą NIH’s National Cancer Institute. NIH nie popiera ani nie rekomenduje żadnych produktów, usług ani informacji opisanych lub oferowanych tutaj przez Healthline. Ostatnia aktualizacja strony 22 czerwca 2016 r.

.jpg)
.jpg)